
دوتریوم
From Wikipedia, the free encyclopedia
دوتریوم (به انگلیسی: Deuterium)، یا هیدروژن سنگین همان عنصر هیدروژن است که علاوه بر پروتون یک نوترون نیز درون هستهٔ آن وجود دارد. در ترکیب با اکسیژن و تشکیل آب اگر مولکول آب توسط دوتریم تشکیل شود به آن آب سنگین میگویند. درهستهٔ هیدروژن سبک نوترون وجود ندارد. در هر لیتر از آب دریا نزدیک به (۳۵) میلیگرم دوتریم وجود دارد. دوتریم یکی از پایههای لازم برای همجوشی هستهای است. در آب در کنار هر ۶۴۲۰ اتم هیدروژن ۱ اتم دوتریم موجود است که تقریباً برابر ۰٫۰۱۵۶٪ است. جدا کردن آن با توجه به نزدیکی خواص آب سنگین و آب سبک بسیار سخت است.
برای تأییدپذیری کامل این مقاله به منابع بیشتری نیاز است. |
 | |
| عمومی | |
|---|---|
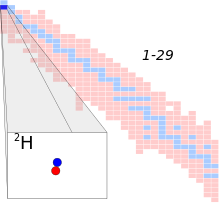
| نماد | ۲H or D |
| نامها | دوتریوم، H or D-۲، deuterium |
| پروتونها | ۱ |
| نوترونها | ۱ |
| اطلاعات هسته | |
| فراوانی طبیعی | ۰٫۰۱۵۶٪ (در زمین) |
| جرم ایزوتوپ | ۲٫۰۱۴۱۰۱۷۸ u |
| اسپین | ۱+ |
| انرژی مازاد | ۱۳۱۳۵٫۷۲۰± ۰٫۰۰۱ keV |
| انرژی بستگی | ۲۲۲۴٫۵۲± ۰٫۲۰ keV |
| ایزوتوپهای جدول کامل نوکلیدها | |
این دوتریمها باید تغلیظ و انبار شوند تا ابتدا به آب سنگین ۱۵ ٪ و سپس به آب ۹۹ ٪ تبدیل شود، جداسازی آب سنگین از آب سبک کاری بسیار سنگین، پیچیده و سخت است. با این همه با توجه به حجم آب در طبیعت دوتریم به اندازهٔ کافی در دریاها برای تأمین نیاز میلیاردها نفر وجود دارد و جهان صنعت کمبودی در این زمینه ندارد.