
Metán
chemická zlúčenina / From Wikipedia, the free encyclopedia
Metán (iné názvy: bahenný plyn, banský plyn, zemný plyn, ľahký uhľovodík [1], traskavý plyn[2], karbán [3], metylhydrid) je najjednoduchší uhľovodík. Je to pri bežných podmienkach bezfarebný plyn s chemickým vzorcom CH4. Čistý metán je bez zápachu, ale na komerčné účely sa zvykne zmiešavať s malým množstvom silno zapáchajúcich zlúčenín síry ako napríklad tetrahydrotiofén/THT/, ktoré mu dodávajú typický zápach, aby sa tak dali zistiť prípadné úniky. Metán tvorí podstatnú časť zemného plynu (až 97 %). Ako plyn vybuchuje v relatívne malom intervale koncentrácie so vzduchom (5 - 15 %).
| Metán | |||||||||||||||||||
 | |||||||||||||||||||
 | |||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||
| Sumárny vzorec | CH4 | ||||||||||||||||||
| Synonymá | bahenný plyn, zemný plyn, banský plyn, metylhydrid, ľahký uhľovodík | ||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||
| Molekulová hmotnosť | 16,04 g/mol | ||||||||||||||||||
| Teplota topenia | -182,5 °C /90,65 K | ||||||||||||||||||
| Teplota varu | -161,6 °C /111,55 K | ||||||||||||||||||
| Trojný bod | -182,48 °C 0,117 bar | ||||||||||||||||||
| Kritický bod | -82,6 °C 46 bar | ||||||||||||||||||
| Teplota vzplanutia | -188 °C | ||||||||||||||||||
| Medze výbušnosti | 5% - 15% | ||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||
| Skupenské teplo topenia | 1,1 kJ/mol | ||||||||||||||||||
| Skupenské teplo vyparovania | 8,17 kJ/mol | ||||||||||||||||||
| Štandardná zlučovacia entalpia | -74,87 kJ/mol | ||||||||||||||||||
| Štandardná entropia | 188 J/mol.K | ||||||||||||||||||
| Merná tepelná kapacita | 35,69 J/mol.K | ||||||||||||||||||
| |||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||
| Číslo CAS | 74-82-8 | ||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||
| Vlastnosti | NIST WebBook | ||||||||||||||||||
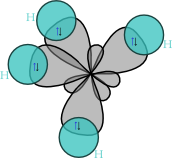
Väzobné uhly v metáne majú veľkosť 109,5 stupňov. Spálenie jednej molekuly metánu za prítomnosti kyslíka uvoľní jednu molekulu oxidu uhličitého (CO2) a dve molekuly vody (H2O):
- CH4 + 2O2 → CO2 + 2H2O
Relatívne vysoký výskyt metánu a čisté spaľovania ho robia veľmi atraktívnym palivom. Avšak keďže za normálnych podmienok to je plyn, je ťažké ho prepravovať z miest, kde sa vyskytuje na miesta, kde je potrebný. Aktívny výskum sa venuje premene metánu na deriváty, ktoré sa dajú prepravovať ľahšie, ako napr. metanol. Niektoré mikroorganizmy nám v tejto selektívnej oxidácii môžu pomôcť produkciou enzýmov nazývaných metánové monooxigenázy.
Metán je relatívne potentný skleníkový plyn s vysokým potenciálom globálneho otepľovania (t. j. efekt globálneho otepľovania porovnaný s oxidom uhličitým).[4] Tretia hodnotiaca správa IPCC konštatuje, že v priemere za 100 ročné obdobie každý kilogram metánu oteplí Zem 25-krát viac ako rovnaké množstvo oxidu uhličitého. Štvrtá hodnotiaca správa sa už opravila berúc do úvahy i nepriame účinky a hovorí, že relatívny faktor otepľovania CH4 k CO2 v priemere za 20 rokov je až 72.[5] Dôvod tejto odlišnosť je fakt, že metán sa v atmosfére časom oxiduje na oxid uhličitý a vodu s polčasom rozpadu sedem rokov.
Doteraz sa odhaduje podiel metánu na globálnom otepľovaní asi na jednu tretinu efektu oxidu uhličitého. Je tu však veľké, doteraz neznáme, množstvo metánu vo forme metánového ľadu na oceánskom dne. Globálne otepľovanie by teoreticky mohlo tento metán uvoľniť, a tak spôsobiť ďalšie oteplenie. Podobné uvoľnenie metánu mohlo byť v minulosti príčinou veľkých vyhynutí na Zemi. Zemská kôra tiež obsahuje veľké množstvá metánu. Veľa metánu sa produkuje aj anaeróbne metánogenézou. Ďalšie zdroje zahŕňajú bahenné sopky spojené s hlbokými geologickými zlomami.



