Disiarczek żelaza(II)
związek chemiczny / Z Wikipedii, wolnej encyclopedia
Disiarczek żelaza(II), FeS
2 – nieorganiczny związek chemiczny z grupy wielosiarczków, zawierający żelazo na II stopniu utlenienia[2]. Anionem jest disiarczek, S2−
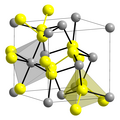
2, w którym atomy siarki połączone są wiązaniem pojedynczym. Występuje naturalnie jako piryt, markazyt i in.[1] Struktura pirytu przypomina chlorek sodu, NaCl, gdzie atomy żelaza zajmują miejsca atomów sodu, a grupy S
2 miejsca atomów chloru, przy czym układ S−S nie jest równoległy do żadnej osi komórki elementarnej[3][4]. Struktura markazytu jest podobna, ale mniej regularna[3] i bywa określana jako wariant rutylu (TiO
2)[4]. Piryt jest jednym z najpowszechniej występujących minerałów siarki i jest najważniejszym źródłem siarki w przemyśle[5].
| |||||||||
 Kryształy pirytu | |||||||||
| |||||||||
| Ogólne informacje | |||||||||
| Wzór sumaryczny |
FeS2 | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
119,97 g/mol | ||||||||
| Minerały | |||||||||
| Identyfikacja | |||||||||
| Numer CAS | |||||||||
| PubChem | |||||||||
Można go otrzymać np. przez ogrzewanie Fe
2O
3 z H
2S[6] lub FeS z H
2S lub z siarką[7]:
- 8FeS + S
8 → FeS
2 - FeS + H
2Saq → FeS
2 + H
2↑
Jest związkiem bardzo trwałym w normalnych temperaturach[6]. Podczas prażenia na powietrzu rozkłada się z wydzieleniem dwutlenku siarki, SO
2[6][8]:
- 4FeS
2 + 11O
2 → 2Fe
2O
3 + 8SO
2↑,
który jest wykorzystywany do produkcji kwasu siarkowego[8].
Natomiast jeżeli prażenie odbywa się bez dostępu powietrza, siarka w FeS
2 ulega dysproporcjonowaniu[6][9]:
- 2FeS
2 → 2FeS + S
2↑