Trijodek azotu
związek chemiczny / Z Wikipedii, wolnej encyclopedia
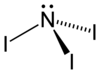
Trijodek azotu, NI
3 – nieorganiczny związek chemiczny azotu i jodu.
Szybkie fakty Nazewnictwo, konst. ...
| |||||||||||||
| |||||||||||||
| Ogólne informacje | |||||||||||||
| Wzór sumaryczny |
NI | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
394,72 g/mol | ||||||||||||
| Wygląd |
ciemnoczerwone ciało stałe | ||||||||||||
| Identyfikacja | |||||||||||||
| Numer CAS | |||||||||||||
| PubChem | |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Podobne związki | |||||||||||||
| Inne aniony |
NCl | ||||||||||||
| Inne kationy |
PI | ||||||||||||
| |||||||||||||
Zamknij
Czysty trijodek azotu jest w warunkach normalnych ciemnoczerwonym ciałem stałym. Czysty NI
3 po raz pierwszy został uzyskany w 1990 roku w wyniku reakcji azotku boru z roztworem fluorku jodu (otrzymanym in situ z ciekłego fluoru i jodu) w trichlorofluorometanie w temperaturze −30 °C i wyizolowany po usunięciu rozpuszczalnika przez sublimację w −20 °C[1]:
- BN + 3IF → NI
3 + BF
3
Jest związkiem bardzo nietrwałym i rozkłada się szybko w postaci czystej i w roztworze w 0 °C, stopniowy rozkład następuje również w −78 °C, trwały jest dopiero w −196 °C[1].